ÉDITION SPÉCIALE MYÉLOME
60TH ASH ANNUAL MEETING
1 au 4 décembre 2018, San Diego, États-Unis
Quoi de mieux que Maia ?
D’après la communication orale de Facon T. et al. Phase 3 Randomized Study of Daratumumab Plus Lenalidomide and Dexamethasone (D-Rd) Versus Lenalidomide and Dexamethasone (Rd) in Patients with Newly Diagnosed Multiple Myeloma (NDMM) Ineligible for Transplant (MAIA).
Late breaking abstract 2 – 60th American Society of Hematology (ASH) Annual Meeting, San Diego, Décembre 2018.
L’étude MAIA, phase 3 randomisant revlimid dexaméthasone, l’un des traitements actuels de référence chez les patients avec un myélome multiple symptomatique en première ligne non éligibles à un traitement intensif depuis l’étude FIRST, versus daratumumab revlimid dexaméthasone a été présenté pour la première fois lors de la session des « late breaking abstract ».
On ne rappelle plus les multiples effets anti-tumoraux directs et indirects du daratumumab, son efficacité notamment en association ayant déjà été démontré dans l’étude POLLUX (revlimid dexaméthasone +/- daratumumab en situation de rechute d’un myélome : survie sans progression passant de 17,5 mois à 44,3 avec l’ajout du daratumumab).
Cette étude internationale a permis l’inclusion de 368 patients dans le bras standard Rev Dex (Rev 25 mg PO de J1 à J21, dexaméthasone 40 mg/semaine ou 20 mg si sujets âgés ou comorbidités ; J1=J21), jusqu’à progression contre le même traitement associé au daratumumab (n=369) 16 mg/kg IV hebdomadaire du cycle 1 et 2, puis tous les 15 jours de C3 à C6 puis tous les 4 semaines jusqu’à progression. L’objectif primaire était la survie sans progression.
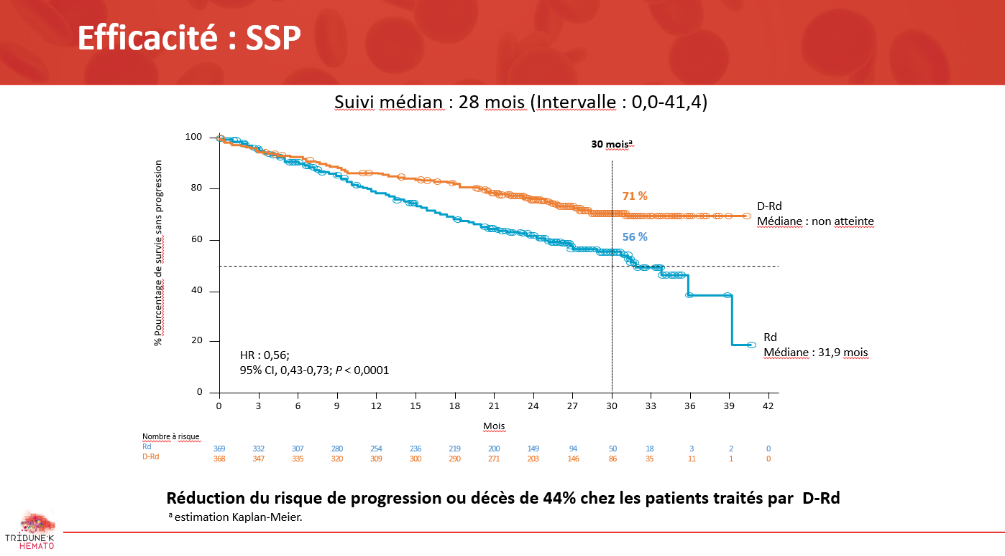
Les résultats de l’analyse intermédiaire ont été présentés lors ce de 60ème ASH. Il est important de préciser que dans cette étude 44 % des patients étaient âgés de plus de 75 ans. Après un suivi médian de 28 mois, la survie sans progression était de 71 % dans le bras Dara Rev Dex contre 56 % dans le bras Rev Dex (HR : 0,56 ; IC 95% : 0,43-0,73 ; p < 0,0001) (Figure 1). Le bénéfice du daratumumab a été retrouvé dans tous les sous-groupes à l’exception des patients de haut-risque cytogénétique (HR : 0,85 (0,44-1,65)). Cette différence de survie sans progression était associée à une augmentation du taux de réponse globale : 93 % contre 81 % dont plus de 48 % de RC ou mieux dans le bras avec Dara et 24 % de patients en MRD négative (contre 7 % dans le bras Rev Dex, p < 0,0001).
Comme attendu suite aux études précédentes la tolérance de cette association était excellente.
Dara Rev Dex : Nouveau standard de traitement en première ligne pour les patients inéligibles à une autogreffe ? Les paris sont ouverts pour la médiane de SSP du bras Dara !
Alexis Talbot